Плътност на течен азот
Плътност на течния азот и другите му физични свойства
В твърдо състояние това са бели кристали.
Азотът е слабо разтворим във вода (по-лош от кислорода), но в същото време е лесно разтворим в течен серен диоксид.
Химичният състав и структурата на течната азотна молекула
При нормални условия азотът е безцветен газ, съставен от молекули N2. Между азотните атоми в молекулата има тройна връзка, в резултат на което нейната молекула е изключително силна. Молекулярният азот е химически неактивен, слабо поляризиран.
Нека разгледаме образуването на азотна молекула (фиг. 1), чийто електронен облак има формата на удължена фигура осем. С приближаването на два азотни атома електронните им облаци се припокриват. Това припокриване е възможно само когато електроните имат антипаралелни завъртания. В областта на припокриващи се облаци електронната плътност се увеличава, в резултат на което силите на привличане между атомите се увеличават. Броят на общите електронни двойки в азотната молекула е равен на един (по един електрон от всеки атом). В молекулата се реализира ковалентен (неполярен) тип връзка.
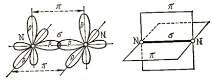
Фигура: 1. Структурата на азотната молекула.
Обобщение на химичните свойства и плътността на течния азот
При нормални условия азотът е химически пасивен елемент; не реагира с киселини, основи, амонячен хидрат, халогени, сяра. Той реагира в незначителна степен с водород и кислород под действието на електрически разряд (1, 2). В присъствието на влага той реагира с литий при стайна температура (3). Реагира с магнезий, калций, алуминий и други метали при нагряване (4, 5, 6).
Реакциите на взаимодействие на азот с флуор и въглерод, както и в случай на водород или кислород, протичат под действието на електрически разряд:
При нагряване до температура 500-600 o C, азотът реагира с литиев хидрид (7), но ако температурният диапазон е 300-350 o C, тогава е възможна реакция с калциев карбид (8):
- Думата UNCOMPRESSOR - Какво е UNCOMPRESSED Значения на думата, примери за употреба
- Думата СТАРО - Какво е СТАРО Значения на думата, примери за употреба
- Думата на WALTORN - Какво е WALTORNA Значения на думата, примери за употреба
- Думата БРИГАДА - Какво е БРИГАДА Значения на думите, примери за употреба
- Думата ДИАТЕЗА - Какво е ДИАТЕЗА Значения на думите, примери за употреба