Метална конструкция
Метали под микроскоп
Всички метали са съставени от огромен брой кристални зърна, които са свързани помежду си. Такава гранулирана кристална структура на веществото може да се види с помощта на специални микроскопи, наречени металографски. Те се различават от обичайните по това, че използват метално странично осветление, тъй като металите са непрозрачни и не могат да бъдат осветени отдолу. В такива микроскопи източникът на светлина е разположен така, че част от лъчите да се отразят от повърхността на металите и да попаднат в лещата.
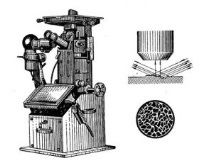
Фигура: 1. Метален микроскоп.
Горе вдясно - светлинните лъчи, отразени от повърхността на тънкия участък, влизат в обектива на микроскопа. Отдолу вдясно - повърхността от чисто желязо, видима с метален микроскоп.
Фигура 1 показва един от тези микроскопи. Преди да разгледате проба в нея, металната повърхност се почиства старателно с шкурка, полира се и се полира до огледално покритие. Такава проба се нарича тънък участък. След това повърхността на тънкия участък се подлага на така нареченото офорт, за което се намокря за 2-3 минути с разтвор, най-често съдържащ азотна киселина и етилов алкохол. Други решения се използват и за офорт на тънки участъци. Те го правят по тази причина: различни зърна от сплавта се разтварят неравномерно с киселина, в резултат на което на повърхността на метала се появяват отделни кристални повърхности и когато осветената част на микросечението се осветява, тогава част от зърната отразява светлината, падаща върху тях директно върху обектива. Тези места изглеждат светлина под микроскопа. Други зърна отразяват светлината отстрани, така че изглеждат тъмни. Под микроскопа местата на адхезия на отделни кристални зърна, така наречените междукристални области, придобиват различен нюанс и равномерен цвят (фиг. 2).
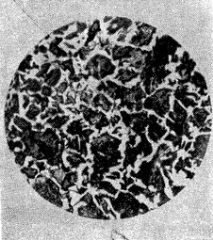
Фигура: 2. Полирана плоча под микроскоп (гравираща стомана с 2% алкохолен разтвор на азотна киселина).
Използването на метален микроскоп даде възможност да се установи каква структура имат металите, как са разположени отделни зърна в сплавта, кои неметални включвания съдържат сплави, отражение на пукнатини на повърхността на сплавите и др. Фигура 3 показва микрофотография от чугун, където отделните включвания на графит са ясно видими.
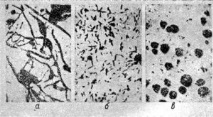
Фигура: 3. Графит в чугун (тъмни включвания):
a-ламеларен графит в обикновен сив чугун; b-фино-ламеларен графит в модифициран сив чугун (модификация 0,15%); n-нодуларни графитни включвания в чугун, модифициран с магнезий (× 100).
Понастоящем металният микроскоп е един от инструментите във всяка лаборатория, където се изследват свойствата на различни метали и сплави.
Кристална решетка от метали
Вече сте запознати с кристалите. Така например, когато изучавате трапезна сол, знаете, че тя се състои от 8 отделни кристала с кубична форма. Самата дума "кристал" идва от гръцката дума "crystallos", което означава "лед". В бъдеще това беше името на всички твърди тела, които имат определена геометрична форма. В природата по-голямата част от твърдите вещества са в кристално състояние. Желязото, като едно от твърдите вещества, също образува кристали, когато се втвърди. Железният кристал има кубична решетка. Въпреки това, гледайки повърхността на метал под микроскоп, няма да видим тази правилна кубична кристална форма. Неправилната форма на кристалите възниква, защото по време на втвърдяването му в стопилката се появяват много малки ядра, които образуват по-големи кристали. Тези големи кристали, сблъсквайки се, започват да се притискат, притискат един друг. Следователно огромно количество кристали се откриват едновременно в втвърдяващия се слитък на метала. Нарушаването на формата им се улеснява не само от факта, че те се бутат един друг, но и от неравномерната температура в различните места на охлаждане. Отделните кристални зърна в втвърдения метал имат различни форми и размери. Те са разделени един от друг със слой, който се състои от различни неметални включвания. Тези неметални включвания винаги присъстват в едно или друго количество в метала.
Метална конструкция
Фигура 4 показва диаграма на формирането на гранулираната структура на метала по време на неговото втвърдяване.

Фигура: 4. Схема на растеж на кристали в втвърдяваща се стопилка:
а - образуват се ембриони; b-кристалите растат; B-кристалите започват да се притискат един към друг; z-отделните зърна се снаждат.
Веществата, които изграждат стоманата, имат различни точки на топене и следователно втвърдяване. Например, чистото желязо става твърдо вече при температура 1539 ° C, а в комбинация със сяра или други елементи температурата на втвърдяване е по-ниска. Следователно металният слой, който се втвърдява на първо място, се състои от най-огнеупорните елементи, например желязо и въглерод. Примесите като сяра и фосфор дават по-ниско топящи се сплави и се втвърдяват последни. Сярата и фосфорът са вредни примеси, тъй като тяхното присъствие значително намалява якостта на сплавта, прави я чуплива и неподходяща за продукти.
Когато сплавта се втвърди, в горната част на слитъка се концентрират по-ниско топими съединения на желязо със сяра и фосфор и се втвърдяват последни, следователно в горната част на слитъка се събира сплав от желязо с фосфор и сяра.
В кристалите атомите на всеки метал се разпределят в строго определен ред. Те образуват така наречената пространствена решетка, която не може да се види с нито един от съществуващите микроскопи. С помощта на рентгенови апарати и други съвременни устройства обаче може да се изследва разположението на атомите в кристалната решетка.
Видове кристални решетки на метали
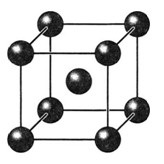
Сред металите най-често се срещат три вида решетки, до първо от които са с кубично телесно центриране. Те се характеризират с факта, че атомите в тях са разположени във върховете и центъра на куба, например в литий, хром, ванадий и други метали (фиг. 5, а).
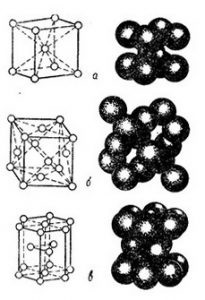
Фиг. 5. Видове метални кристални решетки:
в-шестоъгълна (плътна опаковка).
Да се вторият тип включват лицево центрирана кубична решетка (фиг. 5.6), атоми в (които са разположени на върховете на куба и неговите повърхности (например в алуминий, мед, олово, никел, злато, сребро и платина).
Трети тип - това са шестоъгълни или шестоъгълни, плътно натъпкани решетки (фиг. 5, в). Те се намират в магнезий, цинк, кадмий и берилий.
Както може да се види от диаграмата, показана на фиг. 6, най-плътните уплътнения на атомите имат лице-центрирани и шестоъгълни решетки.

Фиг. 6. Диаграма на металната конструкция.
Решетъчните места са положително заредени йони. В процепа има свободни електрони.
Интересно е да се отбележи, че някои метали, по-специално желязо, цинк и никел, могат да съществуват в няколко кристални форми, преминавайки от една в друга. Този преход се случва при различни температури. Такива модификации, когато едно и също вещество могат да бъдат в различни кристални форми, се наричат алотропни, а самите вещества са алотропни. Името "алотропия" идва от гръцките думи "allos" - друго, "tropos" - свойство.
Въглеродът може да се появи естествено под формата на графит и диамант и както си спомняте, графитът е меко вещество, което оставя следа върху хартията, докато диамантът е едно от най-твърдите вещества в природата. Точките на топене на диаманта и графита са различни.
Алотропната модификация на сярата (ромбична и призматична) е известна. Ромбичната сяра се образува при температури под 96 ° C, над тази температура тя става призматична. В зависимост от промяната в кристалната структура се променят и свойствата на веществото.
Същите алотропни промени се наблюдават и при желязото. Той има решетка от центриран куб при температура 910 ° C, а в температурния диапазон 910-1390 ° C преход към лицево центрирано.
Алотропните трансформации на метал могат лесно да се наблюдават на примера на калай. Обикновеният сребристо-бял калай има сложна кристална решетка, която е стабилна при температури над 18 ° C; при по-ниска температура атомите на калай в кристалите започват да се пренареждат. Опаковката от тях (атоми) става по-малко здрава, лъскавият калай губи своя блясък, ковкост и се превръща в чуплив сив калай с различна кристална решетка.
Това явление беше забелязано отдавна и получи името „калайна чума“, тъй като оловни предмети - калаени чинии, бокали, органи в църквата - понякога изведнъж започват да рушат. Калаената чума беше голямо бедствие. Те не знаеха как да се справят с него, защото не знаеха причините за произхода му. Сега ни е ясно, че ако парче калай се нагрее, „болно от калайната чума“, кристалите от сив калай ще бъдат пренаредени в кристали от бял калай и той отново придобива ковкост и бял цвят.
Метална конструкция
На диаграмите на кристалите (фиг. 5), обикновено в кристалната решетка, се изчертават линии, свързващи един метален атом с друг. В действителност няма линии, свързващи атомите в решетъчните места. Те са опаковани плътно, докосвайки се един друг. Местата на решетката съдържат положително заредени йони, заобиколени от електрони. Валентните електрони на металните атоми, както и самите атоми, са в непрекъсната вибрация. Но външно електроните (валентността) могат по-лесно да напуснат атома си и да отидат към съседния. Следователно, в кристалната решетка има така наречените свободни електрони или свободен електронен „газ“, присъщ на целия комплекс от атоми. По този начин има взаимодействие на електроните на външните обвивки на металните атоми. Благодарение на това външно взаимодействие на електроните се създава връзка между металните атоми и възникват сили на сцепление, които здраво задържат металните атоми в кристалната решетка (фиг. 6). Йони на метални атоми в кристалната решетка, заобиколени от подвижни (нефиксирани) електрони, се наричат йонни атоми, за разлика от обикновените йони.
Това, което казахме за кристалната решетка на металите, се отнася до чисти метали, но знаем, че на практика се използват предимно сплави.
- Структурата на кръвоносната система при различни класове животни
- Структурата на берилиевия атом (Be), диаграма и примери
- ФИЗИЦИТЕ НАМЕРИХА МЕТАЛ, В КОЙТО ЕЛЕКТРОНИТЕ СА КАТО ВОДА
- Физиците са открили метал, електроните в който се държат като вода - РИА Новости
- Точка на топене на металната температура на масата в градуси, при които металът, желязото се топи,