Извличане на суровини от морска вода
НАТРИЕВ ХЛОРИД
Тъй като натриевият хлорид е най-разпространеното вещество, разтворено в морската вода, не е изненадващо, че значително количество (приблизително 4,1010 кг годишно) чист натриев хлорид се получава от морската вода. За тази цел морската вода се филтрира и след това се оставя да се изпари, докато концентрацията на NaCl, който се съдържа, надвиши нейната разтворимост. Твърдият NaCl, който кристализира от морска вода, се оказва доста чист, но може да се прекристализира от прясна вода до още по-висока степен на чистота в зависимост от по-нататъшната употреба.
БРОМ
Повече от 2,3 х 108 кг бром се получават годишно по света, главно от морска вода. Концентрацията на бромиден йон в морската вода е само 8.3.10 –4 М. На първия етап на екстракция на бром от морската вода към нея се добавя сярна киселина, която понижава рН до 3.5. След това хлорният газ се издухва през подкислената вода в известен излишък в сравнение със съдържащия се в него бром. Редокс реакцията протича между хлорния газ, разтворен във вода, и бромидния йон:
C12 (aq.) + 2Br (aq.) = Br2 (aq.) + 2C1 (aq.)
За извличане на бром от морска вода той се прекарва през специална кула, облицована с дървени решетки; въздухът се издухва през кулата в обратна посока. За да се отдели брома от въздушния поток, преминал през кулата, той се обработва със серен диоксид SO2 и пара. В резултат на това се образуват бромоводородна и сярна киселини:
SO2 (r.) + Br2 (g.) + 2H2O (l.) = 2HBr (aq.) + H2SO4 (aq.)
За да се възстанови брома от този разтвор, той отново се обработва с точното количество хлор и след това брома се отстранява чрез продухване с въздух. След това смес от газообразен бром с въздух се прекарва върху студена повърхност. Точката на кипене на течния бром е 59 ° C, което му позволява да се отдели от водата чрез дестилация. Разредената сярна киселина, останала след отстраняване на бром, се използва за подкисляване на пресния прием на морска вода.
МАГНЕЗИЙ
Магнезият е вторият най-разпространен метален елемент в морската вода. Най-големият завод за магнезий с морска вода в САЩ е собственост на Dow Chemical Company и се намира във Фрипорт, Тексас. В тази централа Mg2 + се утаява от морската вода в големи седиментационни резервоари (фиг. 1) под формата на Mg (OH) 2 (PR = 1.8.10 -11) чрез добавяне на CaO негасена вар към морската вода.
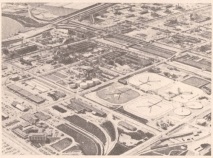
Фигура: 1. Изглед отгоре на утаителните резервоари (в центъра) за утаяване на магнезиев хидроксид от морска вода в заводите на Dow Chemical Company (САЩ). Чертеж от книгата на Т. Браун "Химия в центъра на науките", М, Мир, 1983
Калциевият оксид за този процес от своя страна се получава от черупки на черупчести мекотели. Черупките на ракообразните са съставени от калциев карбонат. Те се измиват, след това се калцинират в специална пещ и по този начин получават негасена вар:
CaCO3 (тв.) = CaO (тв.) + CO2 (g.)
Магнезиевият хидроксид се получава чрез реакция:
Mg2 + (aq.) + CaO (твърдо вещество) + H2O (течност) = Mg (OH) 2 (твърдо вещество) + Ca2 + (aq.)
Утаеният магнезиев хидроксид съдържа примеси на Ca2 +, Na + и HCO3 йони. Твърдата утайка се отфилтрува и след това се обработва със смес от разтвори на НС1 и H2SO4. В кисел разтвор Mg (OH) 2 се разтваря
Mg (OH) 2 (s) + 2H + (aq.) = Mg2 + (aq.) + 2H2O (l.)
Повечето от примесните натриеви йони кристализират в състава на NaCl, а калциевият йон се отлага в състава на CaSO4. Разтворът, съдържащ йони Mg2 +, се филтрира и след това се концентрира в изпарител. По този начин в крайна сметка се получава твърд MgCl2. Той се разтваря в смес от разтопени метални хлориди при 700 ° C в електролизни инсталации (вж. Фиг. 2). Електрическата енергия, подавана към електролизерите, се изразходва за образуването на метален магнезий и газообразен хлор от разтопен магнезиев хлорид:
електричество
MgC12 (g) = Mg (g) + C12 (g)
Разтопеният метал се отлива в блокове, чисти 99,9%.

Фигура: 2. Инсталации за електролитно производство на Mg от MgCl2 в завода на Dow Chemical Company (САЩ). Кръглите вертикални пръти са въглеродни аноди, а правоъгълните пръти са медни проводници, които захранват електролизатори с до 100 000 ампера. Чертеж от книгата на Т. Браун "Химия в центъра на науките", М, Мир, 1983
- Поземлени ресурси и тяхното използване
- Как да осигурим физическата сигурност на корпоративните информационни ресурси
- Отстраняване на счупена подгревна свещ
- ПРЕВОЗ НА ВЪНШНО МОРЕ превод от руски на английски, превод руски на английски
- Как да отбием