Борба с образуването на хидрати в кладенци
Контрол на дебита на газовия кладенец
Дебитът (налягането) се променя с помощта на различни техническифинансови средства:
1) нерегламентирани фитинги, постоянни или недиаметър на колана;
2) регулируеми фитинги;
3) регулатори на налягането;
4) разширителни машини.
Лекция 7
Съхранение на газ в изчерпани или частично изчерпани газови и газокондензатни полета
Изчерпаните газови находища в много случаи се оказахаса най-добрите обекти за създаване на UGS съоръжения в тях, тъй като полето е напълно проучено, геометричноразмер и форма на газоносната зона, геоложки и физически параметри на резервоара, първоначално налягане и температура,превръщане на газ, промяна във времето на дебита на кладенците, коефициенти на филтрационно съпротивление И и IN, режим на полево развитие, технологичен режим на работа, хермеефективност на гумите. Полето разполага с определен запас от довършителни, инжекционни и наблюдателни кладенци, производствени кладенциоръжия за получаване на търговски газ.
Параметри на ПХГ, определени по време на проектирането
1) максиминимално допустимо налягане;
2) минимално необходимото наляганемързел в края на периода на подбор;
3) обеми на активни и буферникрачни газове;
4) броят на инжекционните и производствените кладенци;
5) диаметър m дебелина на стената на полевите и свързващите газопроводи;
6) тип компресорен агрегат за компресорната станция;
7) околомощността на компресорната станция;
8) вида и размера на подземното съоръжение за съхранение за почистване на газ от твърди суспензии по време на инжектирането му в резервоара и сушене по време на екстракция;
9) обемът на допълнителните каподхранващи инвестиции, разходи за съхранение на газ,изплащане на допълнителни капиталови инвестиции.
По време на работа на ПХГ количество обезкървен газ одедаса планирани според графика за разход на газ. Производствени кладенци, необходимо за вземане на проби от газ, се определя, като се вземат предвид среднодневните проби на газ от хранилищетоезера, като подземно хранилище, тревна скала крепостнаситен резервоар, технологичен режим на работа на кладенеца, разположение на кладенците в газоносната зонаност. Необходим брой кладенци и компресори изчислено за двата най-трудни периода на повдигащия храмнишки:
В първия случай максималното изтегляне на газ се извършва при високо налягане, във втория случай разходът на газ, взет от хранилището, е по-малък и налягането на газа в хранилището през този период е минимално.
Лекция
Борба с образуването на хидрати в кладенци
Когато газът се изтегля от резервоара, придружен от намаляване на неговата температура и налягане, водната пара се кондензира и се натрупва в кладенци и газопроводи. При определянеотделни условия, могат да се образуват компоненти на природния газ (метан, етан, пропан, бутан), взаимодействащи с водаграбне нестабилни кристални твърди вещества, наречени хидратами.
Оформен водачплъховете могат да запушат кладенци, газопроводи, сепаратори,унищожи работата на измервателните и контролни устройства. Много често, поради образуването на хидрати, регулаторите на дросела и налягането отказват, дроселът на газ, при който е придружен от рязък спад на температурата. Това нарушава нормалната работа на оборудването на газовото поле.вентилация, особено при ниски температури на околната среда.
Методи за контрол на хидрата може да бъде както предупредителен, така и разрушителен за вече образувани хидрати. За да се унищожат образуваните хидрати в тръбопровода, участъкът от газопровода, където са се образували хидратите, се изключва и газът се освобождава в атмосферата през продухващите тапи, докато налягането в тръбопровода пада и хидратът се разлага. Недостатъкът на този метод е бавното разлагане на хидрата. Не се препоръчва при отрицателни температури, тъй като образуваната вода при отрицателни температури се превръща в ледена запушалка, която може да бъде отстранена само чрез нагряване.
Газовото отопление предотвратява образуването на хидрати, но е ефективно само в полето, тъй като газът бързо се охлажда при движение по тръбопроводи. За да се запази топлината, в някои случаи газопроводите са изолирани.
Когато се въвеждат в газопроводи, повърхностноактивните вещества предотвратяват адхезията (адхезията) на хидратните кристали към стените на тръбите поради образуването на филм върху кристалите, докато кристалите се транспортират с газовия поток.
За да се предотврати образуването на хидрат, газът се изсушава, преди да се подаде в газопровода, използвайки един от съществуващите методи.
Най-ефективният метод за предотвратяване и премахване на образуваните хидрати е доставката на различни хидратни инхибитори.
Като инхибитори се използват алкохоли, електролити и техните смеси - метилов алкохол (метанол), гликоли (етиленгликол EG, диетилен гликол DEG, триетилен гликол TEG, калциев хлорид CaCl2).
В полетата хидратите са най-широко използвани метанол - СНЗОН-което намалява точката на замръзване на водните пари. Образува се метанол, заедно с водни пари, насищащи газанарича алкохолно-водни разтвори, чиято точка на замръзване е значително под нулата. Тъй като количеството водна пара, съдържащо се в газа, намалява, точката на оросяване се понижава и следователно рискът от утаяване на хидрат значително намалява. Метанолът е евтин и не е дефицит. Той е разтворим в алкохоли, смесва се с вода във всякакво съотношение и при смесване с въздух образува взривоопасна смес. Точката на замръзване на метанола е минус 97,1 0 С, плътността е 791 –793 kg/m 3. Метанолът и неговите пари са силно токсични, поради което при работа с метанол трябва да се обърне специално внимание на правилата за безопасна работа.
Метанолът е силна отрова, която действа върху нервната и съдовата система и може да се натрупва в тялото. Отравянето с метанол засяга зрителния нерв и ретината. 5-10 грама причиняват отравяне, ако погълнатите 30 грама са фатални. Вдишването на метанолови пари може да причини припадък, гадене, пиянство и влошено зрение. Поглъщането може да се случи и през кожата. Парите на етилен гликол са токсични, но не са много летливи, така че няма остри отравяния, но са възможни хронични респираторни заболявания.
Консумацията на хидратния инхибитор зависи от количеството влага в газа и количеството на крайното съдържание на влага, при което хидратите не се образуват, както и от концентрацията на добавения и изразходвания инхибитор.
Газохидратите са кристални твърди вещества, които приличат на сняг. Образува се при ниски температури и значително налягане. Кристалните хидрати могат да доведат до запушване на газопровода, поради което той се източва преди подаването на газ в тръбата. Водородният сулфид образува кристални хидрати при температура 0-15 ° C и налягане 0,1-0,5 MPa, необходимо е по-високо налягане за образуването на кристални хидрати CO 2, CH 4 и N 2. Природни газове под формата на твърди хидрати се намират в горната зона на скалите при наличие на ниски температури и достатъчно налягане, по-дълбоки, поради повишаване на температурата, кристалните хидрати вече не могат да съществуват. За образуването на кристални хидрати е необходимо много вода.
Има три възможни начина за образуване на метанхидрат в естествени условия:
1) На мястото на генериране на метан. Веднага след като концентрацията на газ стане достатъчна при дадените термобарични условия, се образуват кристали.
2) На изходи за метан в дъното на басейните.
3) Образуваните газови отлагания в резултат на охлаждане на отделни части от земната кора са в условия, благоприятни за образуването на кристални хидрати. Такива отлагания ще бъдат кристален хидрат (периферията - хидрати, в центъра - свободен газ), най-малките промени в условията на температура и налягане ще доведат до прехода на находището в категорията на прост газ.
Газохидратни находища - прибл. 50% от зоната на РФ, 30% - земя. У нас: Северен Сибир, Тимано-Печорска петролна и газова провинция.
Използването на кристални хидрати: обезсоляване на морска вода, съхранение на газове, разделяне на двойни и многокомпонентни газови и течни смеси, транспортиране на природен газ.
Газохидрати (също хидратира природен газ или клатрати) - кристални съединения, образувани при определени условия на температура и налягане от вода и газ. Името "клатрати" (от лат. clat (h) ratus - „затворено от решетка, засадено в клетка“), е дадено от Пауъл през 1948г. Газохидратите се класифицират като нестехиометрични съединения, т.е. съединения с променлив състав.
За първи път газови хидрати (серен диоксид и хлор) са наблюдавани в края на 18 век от J. Priestley, B. Peletier и V. Karsten. Първите описания на газовите хидрати са дадени от Г. Дейви през 1810 г. (хлорен хидрат). През 1823 г. Фарадей определя приблизително състава на хлорхидрата, през 1829 г. Левит открива бромен хидрат, а през 1840 г. Wöhler получава H2S хидрат. До 1888 г. П. Вилард получава хидрати CH4, C2H6, C2H4, C2H2 и N2O [1] .
Клатратната природа на газовите хидрати е потвърдена през 50-те години. след рентгенови структурни изследвания от Stackelberg и Müller, произведения на Pauling, Claussen.
През 40-те години съветските учени предполагат наличието на газохидратни находища в зоната на вечната замръзналост (Стрижов, Мохнаткин, Черски). През 60-те години те откриват и първите находища на газови хидрати в северната част на СССР. В същото време възможността за образуване и съществуване на хидрати в природни условия намира лабораторно потвърждение (Makogon).
От този момент нататък газовите хидрати се разглеждат като потенциален източник на гориво. Според различни оценки запасите от сухоземни въглеводороди в хидрати варират от 1,8 · 10 5 до 7,6 · 10 9 km³ [2]. Разкрито е широкото им разпространение в океаните и зоните на вечната замръзналост на континентите, нестабилност с повишаване на температурата и намаляване на налягането.
През 1969 г. започва разработването на находището Messoyakhskoye в Сибир, където се смята, че за първи път е било възможно (по чиста случайност) да се извлича природен газ директно от хидрати (до 36% от общия добив към 1990 г. ) [3] .
Хидратите на природния газ сега получават специално внимание като възможен източник на изкопаеми горива, както и като принос за изменението на климата (вж. Хипотезата за пистолета за метан хидрат).
Свойства на хидратите
Хидратите на природния газ са метастабилен минерал, чието образуване и разлагане зависи от температурата, налягането, химичния състав на газа и водата, свойствата на порестата среда и др. [4]
Морфологията на газовите хидрати е много разнообразна. В момента има три основни вида кристали:
- Масивни кристали. Образува се поради сорбцията на газ и вода по цялата повърхност на непрекъснато растящ кристал.
- Мустачки кристали. Те възникват по време на тунелната сорбция на молекулите до основата на растящия кристал.
- Гел кристали. Образува се в обема вода от разтворения в него газ при достигане на условията за образуване на хидрат.
В скалните слоеве хидратите могат да бъдат разпределени под формата на микроскопични включвания или да образуват големи частици, до удължени пластове с дебелина много метри.
Поради своята клатратна структура, единица обем газов хидрат може да съдържа до 160-180 обема чист газ. Плътността на хидрата е по-ниска от плътността на водата и леда (за метан хидрат около 900 kg/m³).
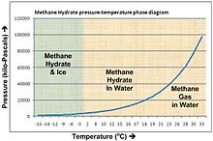
Фазова диаграма на метанхидрат
Тъй като температурата се повишава и налягането намалява, хидратът се разлага на газ и вода, абсорбирайки голямо количество топлина. Разлагането на хидрата в затворен обем или в пореста среда (природни условия) води до значително повишаване на налягането.
Кристалните хидрати имат високо електрическо съпротивление, добра проводимост на звука и практически не пропускат свободни молекули вода и газ. Те се характеризират с аномално ниска топлопроводимост (за метанхидрат при 273 К, пет пъти по-нисък от този за лед).
Теорията на Ван дер Ваалс (внук) - Платтей [5] е широко използвана за описание на термодинамичните свойства на хидратите. Основните разпоредби на тази теория:
- Решетката на гостоприемника не се деформира в зависимост от степента на запълване с гостуващи молекули или от техния тип.
- Всяка молекулярна кухина може да съдържа не повече от една гостуваща молекула.
- Взаимодействието на гост-молекулите е незначително.
- Статистическата физика е приложима към описанието.
Въпреки успешното описание на термодинамичните характеристики, теорията на Ван дер Ваалс - Платте противоречи на данните от някои експерименти. По-специално беше показано, че гост-молекулите са в състояние да определят както симетрията на кристалната решетка на хидрат, така и последователността на фазовите преходи на хидрат. В допълнение е установено силно въздействие на гостите върху молекулите гостоприемници, което води до увеличаване на най-вероятните естествени честоти.
Хидратна структура
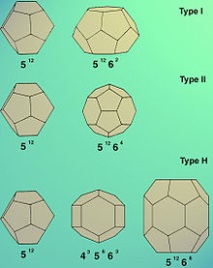
Кристални модификации на газови хидрати.
В структурата на газовите хидрати водните молекули образуват ажурна рамка (т.е. решетката на гостоприемника), в която има кухини. Установено е, че рамковите кухини обикновено са 12- ("малки" кухини), 14-, 16- и 20-хедрони ("големи" кухини), леко деформирани спрямо идеалната форма [6]. Тези кухини могат да бъдат заети от газови молекули („гост молекули“). Газовите молекули са свързани с водната рамка чрез връзки на ван дер Ваалс. Най-общо, съставът на газовите хидрати се описва с формулата MnH2O, където M е молекула на газохидрат-образуващ газ, n е броят на водните молекули на една включена молекула газ и n е променливо число, което зависи относно вида на хидрат-образуващия агент, налягането и температурата.
Кухините, когато се комбинират помежду си, образуват непрекъсната структура от различни видове. Според приетата класификация те се наричат KS, TS, GS - съответно кубични, тетрагонални и шестоъгълни структури. В природата най-често срещаните хидрати от типа KS-I (англ. sI), KS-II (англ. sII), докато останалите са метастабилни.
- Борба с паразитизма в Русия
- Борба дали да не се сменят компенсаторите
- Направи си сам сондаж за кладенец
- 1269-и отделен център за електронна война е
- Algol за аквариум (Algol) инструкции и приложение за борба с водорасли